“유바이오로직스는 높은 기술력이 요구되는 백신 개발에 성공했고, 다양한 백신 파이프라인이 후기 임상 단계에 진입했다. 특히 세균 백신과 바이러스 백신을 개발할 수 있는 플랫폼 기술을 모두 확보했다. 한국의 백신 주권과 보건 안보를 확립하는 데 앞장서겠다.”

유바이오로직스 백영옥 대표의 말이다. 백 대표는 11일 서울 강남구 코엑스에서 열리고 있는 ‘바이오코리아 2023’의 백신 콘퍼런스에서 글로벌 협력을 위한 백신 혁신 기술 사례를 발표했다. 백 대표는 유바이오로직스가 다른 바이오기업과 달리 시판 중인 품목을 여럿 보유, 안정적인 매출을 기반으로 프리미엄 백신 개발을 가속화하겠다고 밝혔다.
실제 유바이오로직스는 지난해 매출 약 550억원을 기록, 2018년 매출 248억원 대비 두배 이상 증가했다. 안정적인 매출과 기술력을 보유한 몇 안 되는 바이오기업 중 하나다. 특히 유바이오로직스는 올해부터 경구용 콜레라 백신 ‘유비콜-플러스’를 유니세프(공공시장)에 독점 공급할 예정이다. 콜레라 백신 공공시장 경쟁사인 샨타 바이오테크닉스(Shantha biotechnics)가 콜레라 백신 생산을 중단하면서 공공시장 물량의 100%를 담당하기로 했다. 매출로는 600억원 규모다.
콜레라는 선진국에선 드물지만, 개발도상국에선 여전히 발병률이 높은 질환 중 하나다. 특히 최근 기후 변화에 따라 가뭄과 홍수가 발생하며, 콜레라 발병률이 증가하는 추세다. 글로벌 시장 조사기관 그랜드뷰리서치(Grand View Research)에 따르면 2020년 기준 콜레라 백신 시장 규모는 1억 달러(약 1329억원)로 추산됐다.

백 대표는 “유바이오로직스는 지속 증가하는 콜레라 백신 수요에 맞춰 제조소 인프라를 확장 중”이라며 “2027년까지 제2공장 증설을 완료해 연간 9000만 도스(Dose)를 생산할 계획”이라고 밝혔다.
유바이오로직스는 강원도 춘천시에 제1공장(C Plant)과 제2공장(V Plant)을 보유하고 있다. 제1공장은 바이러스백신과 세균백신을 생산하고 있고, 케파는 연 2600L 규모다. 제2공장은 세균백신 배양, 정제 라인과 연구 시설을 갖추고 있으며 콜레라 백신의 추가 생산을 하고 있다. 캐파 수준은 연 2750L 규모다.
백 대표는 “유바이오로직스 백신 개발 플랫폼 기술 EuIMT(EuBiologics Immune Modulation Technology)와 EuVCT(EuBiologics Vaccine Conjugation Technology)를 기반으로 파이프라인 확장에 매진 중”이라며 “여러 파이프라인이 임상 후기 단계에 접어든 만큼 괄목할만한 성과가 기대된다”고 전했다.
유바이오로직스는 세균 백신 개발 플랫폼 △EuVCT, 바이러스 백신 개발 플랫폼 △EuIMT와 SNAP(Spontaneous Nanoliposome Antigen Particleization)을 구축했다.
EuVCT는 기존 백신 대비 높은 예방 효과를 위해 특정 세균의 면역원성을 갖는 다당 항원에 전달 단백질(CRM197)을 접합한 기술이다. EuIMT는 신체 면역력을 높이는 기술로 TLR4(Toll like receptor 4)를 촉진시켜 T세포와 B세포 등의 면역세포를 활성화하는 작용을 가진다. 아울러 SNAP는 CoPoP(Cobalt porphyrin Phospholipid, 코발트 포르피린 인지질)을 이용한 리포좀 기반 항원 전달 기술이다. 리포좀 표면에 항원을 붙이게 되면 항원의 면역세포 전달력이 강화돼 면역 효능이 증대된다.
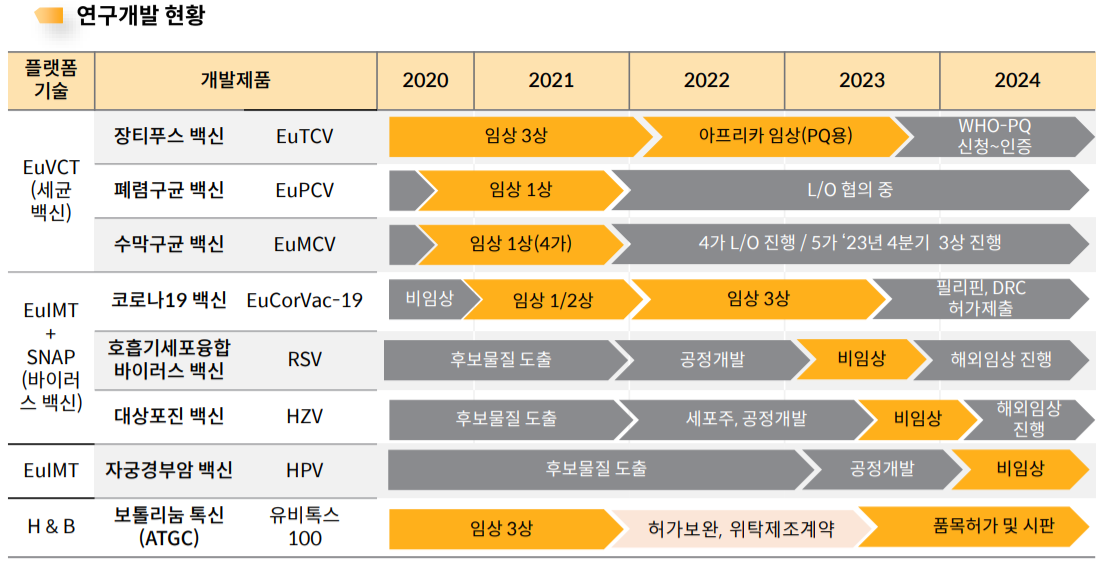
유바이오로직스는 EuVCT를 기반으로 △장티푸스 백신(EuTCV, 3상) △폐렴구균 백신(EuPCV, 1상 완료) △4가 수막구균 백신(EuMCV4, 1상 완료) △5가 수막구균 백신(EuMCV5)을 개발하고 있다.
백 대표는 “장티푸스 백신은 필리핀에서 3상이 완료됐고, WHO-PQ(Prequalification, 사전적격성 평가) 인증을 위해 아프리카에서 임상 3상을 진행 중”이라며 “WHO-PQ는 올해 안에 마무리해 빠르면 내년에는 WHO와 유니세프에 납품할 예정”이라고 말했다. WHO-PQ를 위해선 약 3000명의 대상자 데이터가 필요하다. 유바이오로직스는 임상 3상에서 긍정적인 결과를 바탕으로 WHO-PQ 기준에 충족하기 위한 추가 임상시험을 진행 중이다.
또한 유바이오로직스는 EuIMT와 SNAP를 활용해 △코로나19 백신(EuCorVac-19, 3상) △호흡기세포융합 바이러스 백신(RSV, 전임상) △대상포진 백신(HZV, 전임상) △자궁경부암 백신(HPV, 전임상)을 개발 중이다.
백 대표는 “유코백(코로나19) 백신은 임상 3상이 완료돼, 면역원성 결과를 분석 중”이라며 “상반기 내에 중간결과를 발표할 예정”이라고 밝혔다.
백 대표는 엔데믹에 따라 코로나19 백신의 가치가 없어진 것이 아닌, 독감 백신처럼 매년 지속적인 백신 수요가 전망된다는 입장이다. 특히 유코백이 임상 3상에 성공하면 추후 변이주 대응에는 더욱 신속하게 대응할 수 있고, 콜드체인이 필요한 mRNA 백신과 달리 냉장보관 및 유통이 가능해 개발도상국에서도 사용이 가능한 강점이 있다고 강조했다.
한편 10일 개막한 바이오코리아2023은 13일까지 이어지며, 국내외 기업 간의 파트너링을 포함 전시, 콘퍼런스, 인베스트페어 등 다양한 프로그램이 진행된다.
| 인기기사 | 더보기 + |
-
1 비만치료제 시장, 질주하는 '젭바운드', 위고비에 도전장 -
2 우리나라 신약개발 기술수준 어디쯤? ‘항체치료제’, 美>EU>日>韓>中 순 -
3 영진약품, 셀트리온 '도네리온패취' 국내 단독 유통 및 판매계약 체결 -
4 신풍제약, 영업‧마케팅본부 임직원 대상 CP 교육 개최 -
5 '약국경영대상' ★ 대상 / 서초구 바른온누리약국 / 이혜정약사 -
6 2025년,‘GLP-1 계열’ 최대 매출 품목 ‘등극’ ..비만 '젭바운드' 2배 '껑충' -
7 파로스아이바이오, ‘PHI-101’ ‘PHI-501’ 임상 바탕 기술이전 본격 추진 -
8 [신년특집] K-뷰티의 막강 군단 ‘OEM·ODM’<상> -
9 알피바이오,식물성 다이어트 보조제 ‘시네트롤’ 공급량 56%↑ -
10 한국 제약바이오, 트럼프 2기 정책 변화 속 전략적 대응법은?
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 권혁진 기자 hjkwon@yakup.com
- 입력 2023.05.12 06:00 수정 2023.05.31 18:59
“유바이오로직스는 높은 기술력이 요구되는 백신 개발에 성공했고, 다양한 백신 파이프라인이 후기 임상 단계에 진입했다. 특히 세균 백신과 바이러스 백신을 개발할 수 있는 플랫폼 기술을 모두 확보했다. 한국의 백신 주권과 보건 안보를 확립하는 데 앞장서겠다.”

유바이오로직스 백영옥 대표의 말이다. 백 대표는 11일 서울 강남구 코엑스에서 열리고 있는 ‘바이오코리아 2023’의 백신 콘퍼런스에서 글로벌 협력을 위한 백신 혁신 기술 사례를 발표했다. 백 대표는 유바이오로직스가 다른 바이오기업과 달리 시판 중인 품목을 여럿 보유, 안정적인 매출을 기반으로 프리미엄 백신 개발을 가속화하겠다고 밝혔다.
실제 유바이오로직스는 지난해 매출 약 550억원을 기록, 2018년 매출 248억원 대비 두배 이상 증가했다. 안정적인 매출과 기술력을 보유한 몇 안 되는 바이오기업 중 하나다. 특히 유바이오로직스는 올해부터 경구용 콜레라 백신 ‘유비콜-플러스’를 유니세프(공공시장)에 독점 공급할 예정이다. 콜레라 백신 공공시장 경쟁사인 샨타 바이오테크닉스(Shantha biotechnics)가 콜레라 백신 생산을 중단하면서 공공시장 물량의 100%를 담당하기로 했다. 매출로는 600억원 규모다.
콜레라는 선진국에선 드물지만, 개발도상국에선 여전히 발병률이 높은 질환 중 하나다. 특히 최근 기후 변화에 따라 가뭄과 홍수가 발생하며, 콜레라 발병률이 증가하는 추세다. 글로벌 시장 조사기관 그랜드뷰리서치(Grand View Research)에 따르면 2020년 기준 콜레라 백신 시장 규모는 1억 달러(약 1329억원)로 추산됐다.

백 대표는 “유바이오로직스는 지속 증가하는 콜레라 백신 수요에 맞춰 제조소 인프라를 확장 중”이라며 “2027년까지 제2공장 증설을 완료해 연간 9000만 도스(Dose)를 생산할 계획”이라고 밝혔다.
유바이오로직스는 강원도 춘천시에 제1공장(C Plant)과 제2공장(V Plant)을 보유하고 있다. 제1공장은 바이러스백신과 세균백신을 생산하고 있고, 케파는 연 2600L 규모다. 제2공장은 세균백신 배양, 정제 라인과 연구 시설을 갖추고 있으며 콜레라 백신의 추가 생산을 하고 있다. 캐파 수준은 연 2750L 규모다.
백 대표는 “유바이오로직스 백신 개발 플랫폼 기술 EuIMT(EuBiologics Immune Modulation Technology)와 EuVCT(EuBiologics Vaccine Conjugation Technology)를 기반으로 파이프라인 확장에 매진 중”이라며 “여러 파이프라인이 임상 후기 단계에 접어든 만큼 괄목할만한 성과가 기대된다”고 전했다.
유바이오로직스는 세균 백신 개발 플랫폼 △EuVCT, 바이러스 백신 개발 플랫폼 △EuIMT와 SNAP(Spontaneous Nanoliposome Antigen Particleization)을 구축했다.
EuVCT는 기존 백신 대비 높은 예방 효과를 위해 특정 세균의 면역원성을 갖는 다당 항원에 전달 단백질(CRM197)을 접합한 기술이다. EuIMT는 신체 면역력을 높이는 기술로 TLR4(Toll like receptor 4)를 촉진시켜 T세포와 B세포 등의 면역세포를 활성화하는 작용을 가진다. 아울러 SNAP는 CoPoP(Cobalt porphyrin Phospholipid, 코발트 포르피린 인지질)을 이용한 리포좀 기반 항원 전달 기술이다. 리포좀 표면에 항원을 붙이게 되면 항원의 면역세포 전달력이 강화돼 면역 효능이 증대된다.

유바이오로직스는 EuVCT를 기반으로 △장티푸스 백신(EuTCV, 3상) △폐렴구균 백신(EuPCV, 1상 완료) △4가 수막구균 백신(EuMCV4, 1상 완료) △5가 수막구균 백신(EuMCV5)을 개발하고 있다.
백 대표는 “장티푸스 백신은 필리핀에서 3상이 완료됐고, WHO-PQ(Prequalification, 사전적격성 평가) 인증을 위해 아프리카에서 임상 3상을 진행 중”이라며 “WHO-PQ는 올해 안에 마무리해 빠르면 내년에는 WHO와 유니세프에 납품할 예정”이라고 말했다. WHO-PQ를 위해선 약 3000명의 대상자 데이터가 필요하다. 유바이오로직스는 임상 3상에서 긍정적인 결과를 바탕으로 WHO-PQ 기준에 충족하기 위한 추가 임상시험을 진행 중이다.
또한 유바이오로직스는 EuIMT와 SNAP를 활용해 △코로나19 백신(EuCorVac-19, 3상) △호흡기세포융합 바이러스 백신(RSV, 전임상) △대상포진 백신(HZV, 전임상) △자궁경부암 백신(HPV, 전임상)을 개발 중이다.
백 대표는 “유코백(코로나19) 백신은 임상 3상이 완료돼, 면역원성 결과를 분석 중”이라며 “상반기 내에 중간결과를 발표할 예정”이라고 밝혔다.
백 대표는 엔데믹에 따라 코로나19 백신의 가치가 없어진 것이 아닌, 독감 백신처럼 매년 지속적인 백신 수요가 전망된다는 입장이다. 특히 유코백이 임상 3상에 성공하면 추후 변이주 대응에는 더욱 신속하게 대응할 수 있고, 콜드체인이 필요한 mRNA 백신과 달리 냉장보관 및 유통이 가능해 개발도상국에서도 사용이 가능한 강점이 있다고 강조했다.
한편 10일 개막한 바이오코리아2023은 13일까지 이어지며, 국내외 기업 간의 파트너링을 포함 전시, 콘퍼런스, 인베스트페어 등 다양한 프로그램이 진행된다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
